
2026年3月25日,來自上海的A股上市公司邁威(上海)生物科技股份有限公司 Mabwell (Shanghai) Bioscience Co., Ltd. (下稱"邁威生物”)向港交所遞交招股書,擬香港主板掛牌上市。這是繼其於2025年1月6日、2025年8月29日先後兩次遞表失效後的再一次申請。
邁威生物,此前收到中國證監會境外發行上市備案通知書,可發行不超過6266.46萬股境外上市普通股並在香港聯合交易所上市。
邁威生物(688062.SH),於2022年1月18日在A股上市,截至2026年3月25日收市,總市值約人民幣131億元。

 邁威生物招股書鏈接:
邁威生物招股書鏈接:
https://www1.hkexnews.hk/app/sehk/2026/108329/documents/sehk26032501611_c.pdf
主要業務
邁威生物,成立於2017年,作爲一家以藥物研發方面的創新能力以及從藥物發現至商業化銷售的端到端能力而聞名的中國製藥公司,主要專注於自主開發腫瘤和年齡相關疾病藥物,涉及腫瘤、免疫、眼科、骨科等領域。
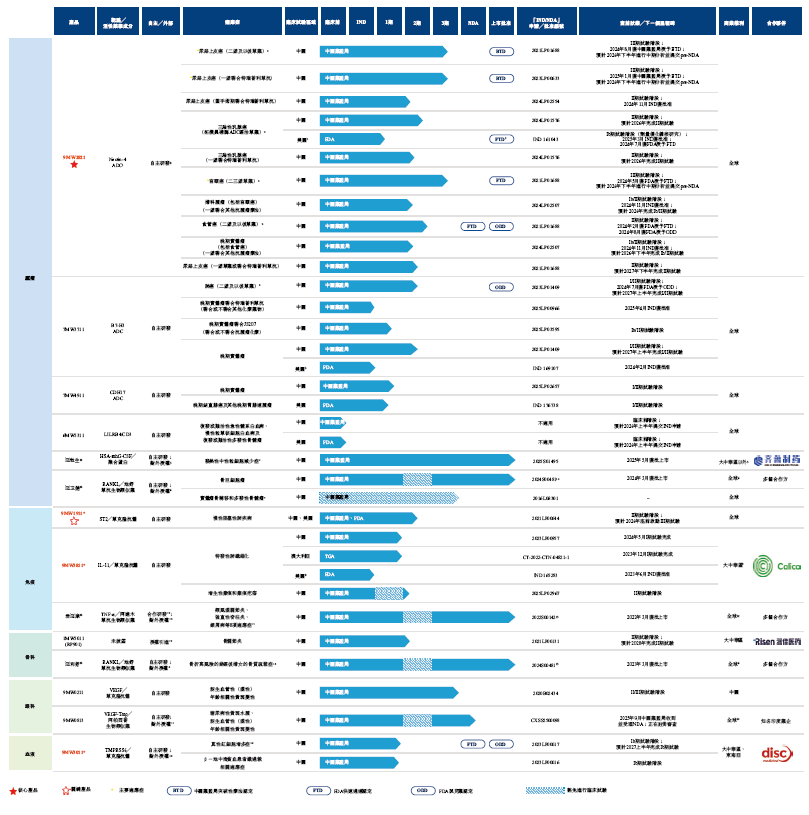
邁威生物,建立的管線產品組合,包括10個以上不同品種的藥物資產,包括:
抗體偶聯藥物ADC
核心產品9MW2821(bulumtatug fuvedotin(BFv),靶向Nectin-4的ADC候選藥物)。目前,就臨床開發階段而言,9MW2821是在中國開發的用於治療尿路上皮癌的所有靶向Nectin-4 ADC中進展最快的,僅次於Padcev。9MW2821也是全球首款進入宮頸癌關鍵III期試驗階段的靶向Nectin-4 ADC。公司正在進行9MW2821的多項臨床試驗,其中包括(i) 9MW2821治療尿路上皮癌的III期試驗,(ii) 9MW2821治療宮頸癌的III期試驗,(iii) 9MW2821治療三陰性乳腺癌的II期試驗;及(iv) 9MW2821治療晚期食管癌的II期臨床試驗;
7MW3711(靶向B7-H3ADC),分別於2023年8月和2023年9月在中國啓動兩項I/II期臨床試驗,以評估7MW3711單藥治療晚期實體瘤的安全性和有效性。此外,於2024年7月,FDA批准了用於治療小細胞肺癌的ODD。於2025年4月,國家藥監局批准公司提交的7MW3711聯合特瑞普利單抗(聯合或不聯合其他化療藥物)治療晚期實體瘤受試者的Ib/II期聯合療法臨床試驗的IND申請。於2026年2月,公司啓動7MW3711聯合JS207或JS207及抗腫瘤療法治療晚期實體瘤患者的Ib/II期臨床試驗。
7MW4911(靶向CDH17 ADC),2025年8月,FDA受理公司開展7MW4911的I/II期臨床試驗的IND申請。2025年10月,7MW4911獲國家藥監局IND批准。2025年11月,公司啓動針對晚期實體瘤患者的I期臨床試驗。2026年1月,公司在美國啓動7MW4911的臨床試驗。
其他差異化模態藥物
9MW3811(一款用於纖維化相關疾病及癌症治療的靶向IL-11的人源化單抗),分別於2023年12月及2024年5月在澳大利亞及中國完成9MW3811針對健康受試者的I期臨床試驗。此外,公司於2023年6月就針對特發性肺纖維化的臨床試驗獲得FDA的IND批准。公司於2025年8月向國家藥監局提交9MW3811針對病理性瘢痕(包括增生性瘢痕和瘢痕疙瘩)臨床試驗的IND申請,國家藥監局於2025年11月授予IND批准,使9MW3811成爲首款進入病理性瘢痕(包括增生性瘢痕和瘢痕疙瘩)治療臨床階段的IL-11靶向藥物。公司於2025年12月啓動9MW3811針對病理性瘢痕(包括增生性瘢痕和瘢痕疙瘩)的臨床試驗。
關鍵產品9MW1911(中國首個獲批進行臨床開發靶向ST2的自主開發候選藥物),於2023年7月在中國啓動針對COPD患者的Ib/IIa期試驗,預期於2026年上半年完成該試驗。於2025年7月在中國啓動針對COPD患者的另一項II期試驗,預期於取得至少120名受試者的52周隨訪數據後進行中期分析,並於2027年下半年完成所有患者隨訪。公司計劃於2026年下半年推進在中國進行的9MW1911治療COPD患者的III期臨床試驗。2025年12月,FDA授予在美國開展9MW1911治療COPD的IIa期臨床試驗的IND批准。
9MW3011(一款重組人源化抗TMPRSS6單抗,爲全球開發狀態領先的靶向TMPRSS6治療藥物),於2024年5月在中國完成針對健康受試者的I期試驗。此外,公司計劃於2027年上半年在中國完成針對真性紅細胞增多症患者的兩項Ib期臨床試驗。
1MW5011(RP901)(一款用於骨關節炎治療的小分子藥物),用於治療膝骨關節炎的II期臨床試驗正在進行患者招募,預計該試驗將於2028年完成。此外,公司於2025年12月啓動治療膝骨關節炎患者的Ib期試驗。
9MW0211(一款重組人源化單克隆抗體,靶向VEGF-A),於2019年5月完成治療眼科疾病的I期試驗。I期試驗結果表明9MW0211具有良好的安全性及療效。公司於2021年5月在中國啓動II/III期臨床試驗,於2025年12月完成該試驗,並計劃於適當時候向國家藥監局提交NDA。
9MW0813(一款重組人VEGF受體- 抗體融合蛋白阿柏西普的生物類似藥),於2024年12月完成9MW0813的III期臨床試驗,並已向國家藥監局提交NDA,NDA已於2025年9月獲受理。
已上市藥物
邁威生物的四款產品君邁康®、邁衛健®(腫瘤)、邁利舒®(骨科)、邁粒生®(發熱性中性粒細胞減少症)已成功上市。
邁威生物的收入來自藥品銷售、對外授權收入。

股東架構
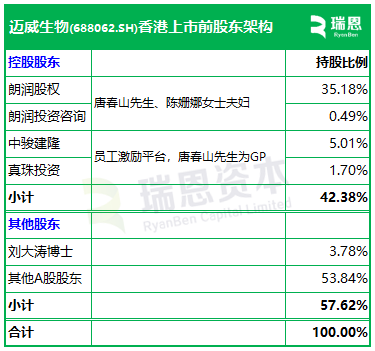
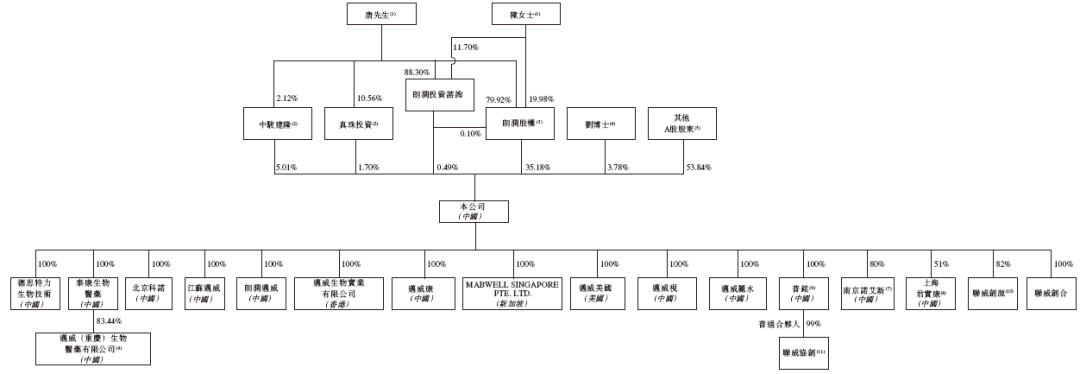
招股書顯示,邁威生物在上市前的股東架構中,
唐春山先生、陳姍娜女士夫婦分別通過朗潤股權、朗潤投資諮詢、中駿建隆(員工激勵平台,唐先生爲GP)、真珠投資(員工激勵平台,唐先生爲GP),分別持股35.18%、0.49%、5.01%、1.74%,合共持股約42.38%。
劉大濤博士,持股3.78%;
其他A股股東,持股53.84%。
董事高管
邁威生物董事會由10名董事組成,包括:
5名執行董事:
唐春山先生(控股股東);
劉大濤博士(董事長、總經理);
武海博士(副總經理兼研發總裁);
胡會國先生(副總經理兼董事會秘書);
桂勳博士(職工代表董事,副總經理);
1名非執行董事:
吳玉鋒先生(海南拾玉私募管理合夥人);
4名獨立非執行董事:
秦正餘先生(紫江企業(600210.SH)首席財務官、副總經理);
許青博士(中國醫藥生物技術協會副理事長);
趙倩博士(上海交通大學醫學院教授);
王芳女士(衡寬國際集團執行董事)。
除執行董事外,高管包括:
王樹海博士(副總經理);
李瀚先生(副總經理);
倪華先生(副總經理);
陳曦女士(副總經理);
華俊先生(副總經理、財務負責人)。
公司業績
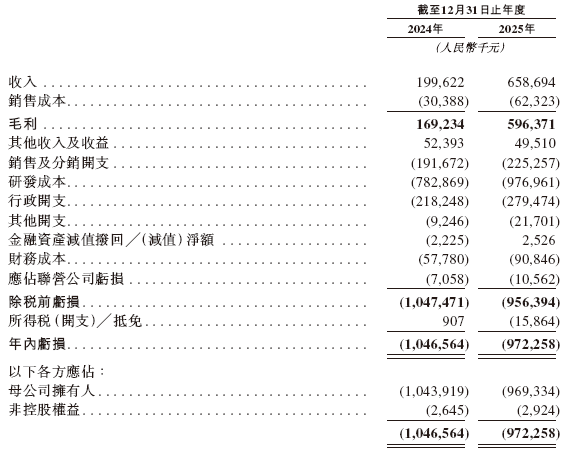
招股書顯示,在過去的2024年和2025年,邁威生物的營業收入分別爲人民幣2.00億和6.59億元,相應的研發開支爲人民幣7.83億和9.77億元,相應的淨虧損分別爲人民幣10.47億和9.72億元。
中介團隊
邁威生物是次IPO的中介團隊主要有:
中信證券、海通國際爲其聯席保薦人;
安永爲其核數師;
競天公誠爲其公司中國律師;
達維爲其公司香港及美國律師;
金杜爲其券商中國律師;
史密夫斐爾爲其券商香港及美國律師;
新百利融資爲其合規顧問;
弗若斯特沙利文爲其行業顧問。
